Los elementos radiactivos son sustancias fascinantes que desempeñan un papel crucial en diversas disciplinas científicas. Desde la medicina hasta la energía nuclear, su estudio no solo nos ayuda a comprender el mundo subatómico, sino que también tiene aplicaciones prácticas que impactan nuestra vida cotidiana.
En este artículo, exploraremos ejemplos concretos de elementos radiactivos, analizando sus propiedades, usos y el impacto que generan. Acompáñanos en esta travesía a través del intrigante universo de la radiactividad.
Contenido
- ### Ejemplos de Elementos Radiactivos: Conociendo sus Características y Usos en la Ciencia y la Industria
- Definición de Elementos Radiactivos
- Ejemplos Comunes de Elementos Radiactivos
- Propiedades Físicas y Químicas
- Aplicaciones de los Elementos Radiactivos
- Riesgos Asociados con la Radiactividad
- Preguntas Frecuentes
### Ejemplos de Elementos Radiactivos: Conociendo sus Características y Usos en la Ciencia y la Industria
Los elementos radiactivos son aquellos que poseen núcleos inestables que se descomponen espontáneamente, liberando radiación en forma de partículas o energía. Estos elementos tienen diversas aplicaciones en la ciencia y la industria, gracias a sus características únicas. A continuación, se presentan algunos ejemplos destacados de elementos radiactivos, así como sus características y usos.
-
Uranio (U)
- El uranio es un elemento pesado que se encuentra en la naturaleza en pequeñas cantidades.
- Se utiliza principalmente como combustible en reactores nucleares debido a su capacidad para mantener reacciones nucleares en cadena.
- El isótopo más común, el uranio-238, tiene una vida media de aproximadamente 4.5 mil millones de años.
-
Plutonio (Pu)
- El plutonio es un elemento sintético que se produce en reactores nucleares.
- Se utiliza en armas nucleares y como combustible en ciertos tipos de reactores.
- Su isótopo más conocido, el plutonio-239, tiene una vida media de 24,100 años.
-
Radio (Ra)
- El radio es un elemento altamente radiactivo que fue descubierto por Marie Curie.
- Se ha utilizado en tratamientos de cáncer mediante terapia radiante, aunque su uso ha disminuido debido a la toxicidad.
- El isótopo más común, el radio-226, tiene una vida media de 1,600 años.
-
Carbono-14 (C-14)
- Este isótopo radiactivo del carbono se utiliza en datación por radiocarbono, lo que permite determinar la edad de restos orgánicos hasta unos 50,000 años.
- El C-14 se forma en la atmósfera y es absorbido por los seres vivos durante su vida.
- Su vida media es de aproximadamente 5,730 años.
-
Tecnicio (Tc)
- El tecnicio es un elemento sintético que no se encuentra en la naturaleza en cantidades significativas.
- Se utiliza en medicina nuclear, especialmente en estudios de imágenes y diagnóstico.
- El isótopo más utilizado es el tecnicio-99m, que tiene una vida media de 6 horas.
Los elementos radiactivos también tienen aplicaciones industriales importantes. Por ejemplo, se utilizan en:
- Radiografía industrial: Utilizan radiación para detectar fallas en materiales y estructuras.
- Medicina nuclear: Diagnóstico y tratamiento de enfermedades.
- Investigación científica: Estudio de procesos biológicos y físicos mediante trazadores radiactivos.
Cada uno de estos elementos presenta características singulares que los hacen útiles en diferentes campos, resaltando la importancia de la radiactividad en nuestras vidas cotidianas y en el avance de la tecnología.
Definición de Elementos Radiactivos
Los elementos radiactivos son aquellos que poseen núcleos inestables, lo que les lleva a emitir radiación en forma de partículas o energía para alcanzar una configuración más estable. Esta emisión puede manifestarse de diferentes modos, como partículas alfa, beta y rayos gamma. La radiactividad es un fenómeno natural que ocurre en ciertos isótopos de elementos químicos, y su estudio ha sido fundamental en diversas aplicaciones científicas y tecnológicas.
La radiactividad se clasifica en dos tipos principales: la radiactividad natural, que se produce de manera espontánea en la naturaleza, y la radiactividad artificial, que es generada por el ser humano a través de procesos nucleares. Los elementos radiactivos naturales, como el uranio y el torio, se encuentran en diversas concentraciones en la corteza terrestre, mientras que los elementos radiactivos artificiales, como el plutonio, son creados en laboratorios o reactores nucleares.
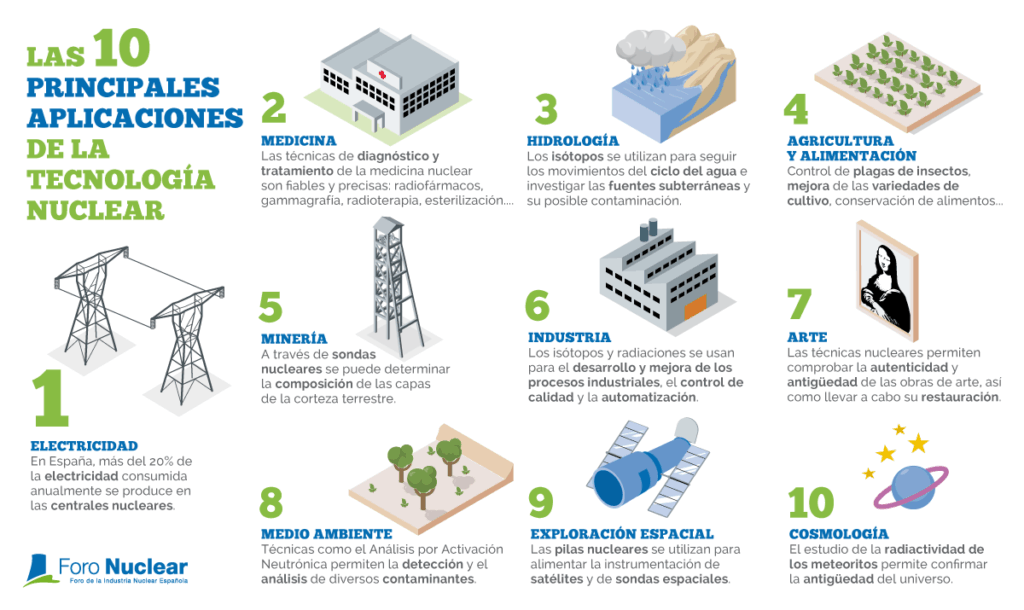
El estudio de estos elementos no solo es relevante por su impacto en la salud humana y el medio ambiente, sino también por sus aplicaciones en campos como la medicina, la energía nuclear y la investigación científica. Por ejemplo, algunos isótopos radiactivos son utilizados en terapias contra el cáncer, mientras que otros son fundamentales en la producción de energía eléctrica mediante reacciones nucleares controladas.
Ejemplos Comunes de Elementos Radiactivos
Entre los elementos radiactivos más comunes, podemos encontrar:
- Uranio (U): Utilizado principalmente como combustible en reactores nucleares.
- Radio (Ra): Empleado en tratamientos médicos y en la investigación.
- Polonio (Po): Utilizado en dispositivos de eliminación de estática.
- Cesio (Cs): Usado en relojes atómicos y en aplicaciones industriales.
Cada uno de estos elementos tiene propiedades únicas y aplicaciones específicas. El uranio, por ejemplo, es crucial en la generación de energía nuclear, ya que su fisión libera grandes cantidades de energía. Por el contrario, el radio ha sido históricamente utilizado en tratamientos de cáncer, aunque su uso ha disminuido debido a los riesgos asociados con la exposición a la radiación.
El polonio, descubierto por Marie Curie, es conocido por su alta radiactividad y su aplicación en la eliminación de electricidad estática en ciertos procesos industriales. Por otro lado, el cesio es famoso por su aplicación en tecnología de precisión, como en la sincronización de relojes atómicos, que son fundamentales para sistemas de navegación y telecomunicaciones.
Propiedades Físicas y Químicas
Los elementos radiactivos presentan propiedades físicas y químicas que los distinguen de otros elementos. En términos físicos, muchos de estos elementos son metales pesados y tienen altos puntos de fusión y ebullición. La mayoría son sólidos a temperatura ambiente, y su densidad suele ser significativamente mayor que la de los elementos no radiactivos.
Desde el punto de vista químico, los elementos radiactivos suelen exhibir comportamientos similares a los de otros metales en su grupo de la tabla periódica. Por ejemplo, el uranio y el torio son actínidos y comparten características como la formación de compuestos oxídicos. Sin embargo, su radiactividad implica que sus interacciones con otros elementos y compuestos pueden resultar en reacciones químicas especiales, que pueden afectar tanto la estabilidad como el manejo seguro de estos materiales.
Es importante señalar que la radiactividad puede influir en las propiedades químicas de los elementos, ya que algunos isótopos pueden ser más reactivos que otros. Además, la presencia de radiación puede provocar cambios en las estructuras moleculares de los compuestos con los que interactúan, lo que puede tener implicaciones en la seguridad ambiental y en la salud pública.
Aplicaciones de los Elementos Radiactivos
Los elementos radiactivos tienen un amplio espectro de aplicaciones en distintas áreas. Algunas de las más destacadas incluyen:
- Energía Nuclear: Utilizados como combustible en reactores nucleares.
- Medicina: Aplicaciones en diagnóstico y tratamiento de enfermedades.
- Investigación Científica: Usados como trazadores y en estudios de datación.
- Industria: Aplicaciones en mediciones y control de calidad.
En el ámbito de la energía nuclear, el uranio y el plutonio son los elementos más comunes utilizados en reactores para la generación de electricidad. Estos procesos permiten la producción de grandes cantidades de energía con una menor emisión de gases de efecto invernadero en comparación con los combustibles fósiles.
En medicina, isótopos radiactivos como el tecnecio-99m son esenciales en la imagenología médica, permitiendo a los médicos realizar exploraciones precisas del cuerpo humano. Asimismo, tratamientos con radioterapia utilizan elementos como el yodo-131 para atacar células cancerosas.
La investigación científica también se beneficia de los elementos radiactivos, ya que se emplean en técnicas de datación, como el carbono-14, que permite determinar la antigüedad de restos orgánicos. En la industria, se utilizan en aplicaciones de control de calidad, como en la medición de espesores de materiales, donde la radiactividad proporciona datos precisos y confiables.
Riesgos Asociados con la Radiactividad
A pesar de sus numerosas aplicaciones, los elementos radiactivos conllevan riesgos significativos para la salud y el medio ambiente. La exposición a la radiación puede causar daños celulares y aumentar el riesgo de desarrollar enfermedades, como cáncer. Por esta razón, es crucial manejar estos materiales con precaución.
La radiación ionizante emitida por elementos radiactivos puede afectar tanto a seres humanos como a organismos vivos en general. Se han documentado efectos agudos, como quemaduras por radiación, así como efectos crónicos, que pueden manifestarse años después de la exposición. La protección de los trabajadores que manipulan estos materiales es fundamental, y se implementan medidas estrictas de seguridad en instalaciones donde se utilizan.
Además, el desecho de elementos radiactivos plantea un desafío importante para la gestión ambiental. Es necesario establecer protocolos adecuados para el almacenamiento y la eliminación de desechos radiactivos, garantizando que no contaminen el entorno. Las estrategias de descontaminación y recuperación de sitios contaminados son igualmente críticas para mitigar los impactos negativos de la radiactividad en el medio ambiente.
En conclusión, aunque los elementos radiactivos son objetos de gran utilidad en múltiples campos, es esencial abordar su manejo con responsabilidad y conocimiento, considerando siempre los riesgos asociados a su uso.
Preguntas Frecuentes
¿Cuáles son los ejemplos más comunes de elementos radiactivos en la naturaleza y sus aplicaciones prácticas?
Los ejemplos más comunes de elementos radiactivos en la naturaleza incluyen el uranio, que se utiliza como combustible en reactores nucleares; el radón, que se mide para evaluar riesgos de salud en viviendas; y el carbono-14, que se emplea en datación de restos orgánicos. Estos elementos tienen aplicaciones prácticas en energía, medicina y arqueología.
¿Cómo se clasifican los elementos radiactivos y qué ejemplos ilustran cada categoría?
Los elementos radiactivos se clasifican en dos categorías principales: naturales y artificiales.
1. Elementos radiactivos naturales: Se encuentran en la naturaleza y su radiactividad proviene de la descomposición de núcleos atómicos inestables. Ejemplos incluyen el uranio-238 y el radio-226.
2. Elementos radiactivos artificiales: Son creados por el ser humano en laboratorios o reactores nucleares. Ejemplos son el cesio-137 y el plutonio-239.
Estos ejemplos ilustran cómo se diversifican los elementos radiactivos según su origen.
¿Qué ejemplos de elementos radiactivos se utilizan en medicina y cuáles son sus beneficios terapéuticos?
Ejemplos de elementos radiactivos utilizados en medicina incluyen el yodo-131 y el tecnecio-99m. El yodo-131 se utiliza en el tratamiento de enfermedades tiroideas, como el hipertiroidismo, ya que ayuda a destruir tejido tiroideo anormal. Por otro lado, el tecnecio-99m es ampliamente empleado en imágenes médicas, permitiendo diagnósticos precisos en diversas condiciones al resaltar áreas específicas del cuerpo durante la exploración. Estos elementos ofrecen beneficios terapéuticos significativos al mejorar la detección y tratamiento de enfermedades.
¿Qué características específicas poseen los ejemplos de elementos radiactivos que los diferencian de otros tipos de elementos químicos?
Los elementos radiactivos se diferencian de otros elementos químicos por su inestabilidad nuclear, que les lleva a desintegrarse y emitir radiación en forma de partículas o rayos. Además, poseen un número atómico alto y suelen tener isótopos con diferentes propiedades radiactivas, lo que no ocurre en todos los elementos. Estas características hacen que sean utilizados en aplicaciones como la medicina y la energía nuclear.
En conclusión, los elementos radiactivos desempeñan un papel crucial en diversas aplicaciones científicas y tecnológicas. Comprender sus características y ejemplos es fundamental para avanzar en campos como la medicina y la energía. Te invitamos a compartir este contenido y seguir explorando más sobre la fascinante ciencia de la radiactividad.