Descubre la fascinante estructura y nomenclatura de las oxisales, compuestos químicos esenciales en la vida cotidiana y en numerosos procesos industriales. En este artículo, exploraremos ejemplos concretos de oxisales que te permitirán comprender su composición y funciones en diversos contextos. Desde el sulfato de cobre hasta el nitrato de potasio, sumérgete en la complejidad y relevancia de estas sustancias. ¡Acompáñanos en este viaje por la química de las oxisales!
Contenido
¿Qué son los oxisales y ejemplos?

Los oxisales son una clase de compuestos químicos que se forman mediante la combinación de un ácido oxo con una base. Un ácido oxo es un ácido que contiene oxígeno, como el ácido sulfúrico (SO4) o el ácido fosfórico (H3PO4). Los oxisales se caracterizan por contener un ión metálico y un ión polioxo, que es un ión que contiene varios átomos de oxígeno unidos a un átomo central.
Estructura y propiedades de los oxisales
Los oxisales tienen una estructura cristalina compleja, en la que los iones metálicos y polioxo se encuentran dispuestos de manera regular. Esta estructura les confiere propiedades interesantes, como una alta estabilidad térmica y resistencia química. Algunos ejemplos de oxisales y sus propiedades son:
- El sulfato de cobre (CuSO4) es un oxisal que se utiliza como fungicida y insecticida.
- El fosfato de sodio (Na3PO4) es un oxisal que se utiliza como detergente y suavizante de agua.
- El cromato de potasio (K2CrO4) es un oxisal que se utiliza como pigmento y inhibidor de corrosión.
Usos de los oxisales en la industria
Los oxisales tienen un amplio rango de aplicaciones en la industria, debido a sus propiedades únicas. Algunos ejemplos de usos de los oxisales son:
- Los oxisales se utilizan como catalizadores en la producción de polímeros y plásticos.
- Los oxisales se utilizan como pigmentos en la producción de pinturas y tintes.
- Los oxisales se utilizan como inhibidores de corrosión en la producción de metales y aleaciones.
Riesgos y precauciones al manejar oxisales
Los oxisales pueden ser tóxicos y corrosivos, por lo que es importante manejarlos con precaución. Algunos ejemplos de riesgos y precauciones al manejar oxisales son:
- Los oxisales pueden causar irritación en la piel y ojos, por lo que es importante usar guantes y gafas al manejarlos.
- Los oxisales pueden ser tóxicos si se ingieren, por lo que es importante evitar su ingestión.
- Los oxisales pueden reaccionar con otros compuestos químicos, por lo que es importante manejarlos en un ambiente controlado.
¿Cómo saber si es un oxisal?
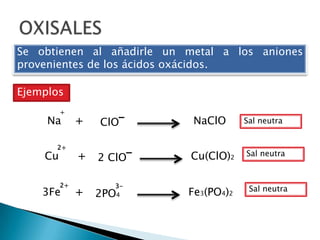
Un oxisal es un tipo de sal que se forma a partir de la combinación de un óxido con un ácido. Para saber si una sustancia es un oxisal, debemos analizar su composición química y buscar ciertas características.
Características generales de los oxisales
Los oxisales suelen tener ciertas características que los distinguen de otros tipos de sales. Algunas de estas características son:
- Suelen ser sólidos a temperatura ambiente.
- Tienen un punto de fusión alto.
- Son solubles en agua, aunque algunos pueden ser insolubles.
Análisis químico de los oxisales
Para determinar si una sustancia es un oxisal, debemos analizar su composición química. Algunos de los métodos que se pueden utilizar son:
- Análisis de espectroscopía: se utiliza para determinar la presencia de ciertos elementos en la sustancia.
- Análisis de difracción de rayos X: se utiliza para determinar la estructura cristalina de la sustancia.
- Análisis de reacciones químicas: se utiliza para determinar la presencia de ciertos grupos funcionales en la sustancia.
Ejemplos de oxisales
Algunos ejemplos de oxisales son:
- Nitratos: son oxisales que contienen el ion nitrato (NO3).
- Sulfatos: son oxisales que contienen el ion sulfato (SO42).
- Carbonatos: son oxisales que contienen el ion carbonato (CO32).
¿Qué son las sales ácidas y ejemplos?

Las sales ácidas son compuestos químicos que se forman a partir de la reacción entre un ácido y una base. Estas sales contienen un cation (ión positivo) y un anión (ión negativo) que proviene del ácido. Las sales ácidas pueden ser clasificadas en diferentes tipos según su composición y propiedades.
Tipos de sales ácidas
Las sales ácidas se pueden clasificar en diferentes tipos según su composición y propiedades. Algunos de los tipos más comunes de sales ácidas son: 1. Sales ácidas orgánicas: Estas sales se forman a partir de la reacción entre un ácido orgánico y una base. Ejemplos de sales ácidas orgánicas son: Acetato de sodio (CH3COONa) Citrato de potasio (C6H5O7K3) Tartrato de sodio (C4H4O6Na2)
2. Sales ácidas inorgánicas: Estas sales se forman a partir de la reacción entre un ácido inorgánico y una base. Ejemplos de sales ácidas inorgánicas son: Cloruro de hidrógeno (HCl) Sulfato de cobre (CuSO4) Nitrato de plata (AgNO3)
3. Sales ácidas complejas: Estas sales se forman a partir de la reacción entre un ácido y una base que contiene un metal de transición. Ejemplos de sales ácidas complejas son: Tetraclorocuprato de sodio (Na2CuCl4) Hexacianoferrato de potasio (K4Fe(CN)6)
Propiedades de las sales ácidas
Las sales ácidas tienen varias propiedades que las caracterizan. Algunas de estas propiedades son: 1. Solubilidad: Las sales ácidas pueden ser solubles o insolubles en agua, dependiendo de su composición y estructura.
2. Conductividad eléctrica: Las sales ácidas pueden ser conductoras de electricidad, ya que contienen iones que pueden moverse libremente.
3. Reactividad: Las sales ácidas pueden reaccionar con otros compuestos químicos, como ácidos o bases, para formar nuevos compuestos.
Ejemplos de sales ácidas en la vida cotidiana
Las sales ácidas se encuentran en muchos productos y procesos de la vida cotidiana. Algunos ejemplos son: 1. Alimentos: Las sales ácidas se utilizan como conservantes y saborizantes en alimentos como la sal de mesa (cloruro de sodio), el vinagre (acetato de etilo) y la mermelada (citrato de sodio).
2. Medicamentos: Las sales ácidas se utilizan en la fabricación de medicamentos, como el cloruro de hidrógeno (HCl) que se utiliza para tratar la acidez estomacal.
3. Industria: Las sales ácidas se utilizan en la industria para la producción de papel, textiles y otros productos.
¿Cómo se nombran las oxisales neutras?

Las oxisales neutras se nombran utilizando un conjunto de reglas establecidas por la Unión Internacional de Química Pura y Aplicada (IUPAC). Estas reglas se basan en la composición química de la sal y en la identidad del metal y del no metal que la componen.
Nomenclatura de las oxisales neutras de metales alcalinos y alcalinotérreos
Las oxisales neutras de los metales alcalinos (como el litio, el sodio y el potasio) y de los metales alcalinotérreos (como el magnesio, el calcio y el estroncio) se nombran utilizando la forma óxido de [nombre del metal]. Por ejemplo:
- La oxisal neutra de litio y oxígeno se llama óxido de litio.
- La oxisal neutra de sodio y oxígeno se llama óxido de sodio.
- La oxisal neutra de calcio y oxígeno se llama óxido de calcio.
Nomenclatura de las oxisales neutras de metales de transición
Las oxisales neutras de los metales de transición (como el hierro, el cobre y el zinc) se nombran utilizando la forma óxido de [nombre del metal] (II) o (III), dependiendo del estado de oxidación del metal. Por ejemplo:
- La oxisal neutra de hierro y oxígeno en estado de oxidación II se llama óxido de hierro (II).
- La oxisal neutra de cobre y oxígeno en estado de oxidación II se llama óxido de cobre (II).
- La oxisal neutra de zinc y oxígeno en estado de oxidación II se llama óxido de zinc.
Nomenclatura de las oxisales neutras de no metales
Las oxisales neutras de los no metales (como el carbono, el nitrógeno y el azufre) se nombran utilizando la forma [nombre del no metal] óxido. Por ejemplo:
- La oxisal neutra de carbono y oxígeno se llama dióxido de carbono.
- La oxisal neutra de nitrógeno y oxígeno se llama óxido de nitrógeno.
- La oxisal neutra de azufre y oxígeno se llama dióxido de azufre.
Ejemplos destacados de Oxisales: ¡Descubre su composición y propiedades!
Las oxisales son un tipo de compuesto químico que se caracteriza por estar formado por iones tanto de átomos de oxígeno como de otro elemento más electropositivo. Estas sustancias son ampliamente utilizadas en la industria y en la vida cotidiana, por lo que es fundamental comprender su composición y propiedades para poder apreciar su importancia en diversos procesos químicos.
Uno de los ejemplos más destacados de oxisales es el sulfato de calcio, cuya fórmula química es CaSO4. Este compuesto es conocido comúnmente como yeso y se utiliza en la construcción, la agricultura y la industria alimentaria. El sulfato de calcio es soluble en agua y presenta propiedades como la capacidad de endurecerse al secarse, lo que lo hace ideal para la fabricación de materiales de construcción.
Otro ejemplo relevante de oxisal es el nitrato de potasio, con fórmula química KNO3. Este compuesto, también conocido como salitre, se emplea en la fabricación de pólvora y fue utilizado históricamente en la industria pirotécnica. El nitrato de potasio es soluble en agua y tiene propiedades oxidantes, lo que lo hace útil en diversas aplicaciones industriales.
Además, no podemos dejar de mencionar el carbonato de calcio, cuya fórmula química es CaCO3. Este compuesto es uno de los minerales más abundantes en la naturaleza y se encuentra en rocas como el mármol y la calcita. El carbonato de calcio se utiliza en la industria química, farmacéutica y alimentaria, destacando por su capacidad de neutralizar ácidos y regular el pH en diferentes procesos.
En cuanto a las propiedades de las oxisales, es importante destacar su capacidad para formar cristales sólidos con estructuras bien definidas, así como su comportamiento frente a la disociación en soluciones acuosas. Estas sustancias pueden presentar diferentes estados de oxidación del átomo central, lo que les confiere una gran versatilidad en sus aplicaciones químicas.
En resumen, las oxisales son compuestos químicos fundamentales en numerosos procesos industriales y en la vida diaria. Su variedad de composiciones y propiedades las convierten en elementos clave en la química y en la ciencia en general. Es necesario profundizar en su estudio para comprender su impacto en nuestra sociedad y en el desarrollo de nuevas tecnologías.
FORMACION DE OXISALES
Propiedades de las Oxisales
Composición química
Las oxisales son compuestos químicos formados por sales que contienen oxígeno en su estructura molecular. Estas sales se componen de un catión metálico y un anión poliatómico que incluye oxígeno, como el ion sulfato (SO4) o el ion nitrato (NO3). La presencia del oxígeno en estas sales confiere propiedades específicas a las oxisales, determinando su comportamiento químico y físico.
Estructura cristalina
Las oxisales suelen presentar una estructura cristalina en la que los iones metálicos y los iones poliatómicos se organizan de manera ordenada en una red tridimensional. Esta estructura cristalina puede variar según el tipo de oxisal, influenciando sus propiedades físicas, como el punto de fusión, la solubilidad y la conductividad eléctrica. La disposición de los iones en la red cristalina también determina la geometría de los cristales de oxisales.
Propiedades químicas
Las oxisales presentan diversas propiedades químicas que las diferencian de otros tipos de sales. Por ejemplo, muchas oxisales son hidrosolubles, es decir, se disuelven en agua formando soluciones acuosas. Esta propiedad se debe a la interacción entre los iones de la oxisal y las moléculas de agua, que favorece la disociación de la sal en sus componentes iónicos. Además, algunas oxisales pueden experimentar reacciones de neutralización al reaccionar con ácidos para formar sales neutras y agua.
Usos y aplicaciones
Las oxisales tienen una amplia variedad de usos y aplicaciones en diferentes campos. Por ejemplo, el sulfato de cobre (CuSO4) se utiliza en la industria agrícola como fungicida y fertilizante, mientras que el nitrato de potasio (KNO3) se emplea en pirotecnia y en la fabricación de explosivos. Las propiedades químicas y físicas de las oxisales determinan su utilidad en diversos procesos industriales, científicos y tecnológicos, convirtiéndolas en compuestos químicos de gran importancia en la sociedad actual.
Preguntas Frecuentes
¿Cuáles son algunas aplicaciones prácticas de las sales oxisales en la industria química?
Algunas aplicaciones prácticas de las sales oxisales en la industria química incluyen su uso como agentes oxidantes, para la fabricación de productos de limpieza y desinfectantes, así como en la producción de fertilizantes agrícolas.
¿Cómo se pueden clasificar y distinguir las sales oxisales en base a su composición química?
Las sales oxisales se pueden clasificar y distinguir en base a su composición química según la presencia de oxígeno y de ácido en su estructura.
¿Qué tipo de reacciones químicas suelen dar origen a la formación de sales oxisales en la naturaleza?
Las reacciones químicas que suelen dar origen a la formación de sales oxisales en la naturaleza son aquellas en las que intervienen ácidos y bases.
¿Cuáles son los principales usos de las sales oxisales en la vida cotidiana y en la investigación científica?
Las sales oxisales se utilizan en la vida cotidiana como condimentos para dar sabor a los alimentos, como abonos para mejorar la calidad de la tierra en la agricultura, y en la industria química para la fabricación de productos diversos. En la investigación científica, las sales oxisales se emplean como reactivos en experimentos y análisis químicos, así como en la síntesis de compuestos de interés.
En conclusión, las oxisales son compuestos químicos de gran importancia en la industria y la vida cotidiana. Su estudio nos permite comprender la estructura y propiedades de estos compuestos. ¡Comparte este artículo para seguir explorando el fascinante mundo de las oxisales! ¡Sigue leyendo y amplía tus conocimientos en Química Inorgánica!