El enlace covalente es fundamental en la química, ya que define cómo los átomos se combinan para formar moléculas. Comprender su estructura de Lewis es esencial para visualizar y predecir el comportamiento de estas sustancias. En este artículo, exploraremos diversos ejemplos que ilustran cómo se representa el enlace covalente a través de diagramas de Lewis, facilitando así un entendimiento profundo de las interacciones atómicas.
Adéntrate en el fascinante mundo de la química y descubre cómo estos conceptos cobran vida en la práctica diaria.
Contenido
- Comprendiendo el Enlace Covalente a través de Ejemplos de Estructura de Lewis
- Definición y Características del Enlace Covalente
- Aplicación de la Estructura de Lewis en la Predicción de Enlaces Covalentes
- Diferencias entre Enlace Covalente Polar e Im polar
- Ejemplos Prácticos de Enlaces Covalentes en Compuestos Comunes
- Conclusiones sobre el Enlace Covalente y la Estructura de Lewis
- Preguntas Frecuentes
Comprendiendo el Enlace Covalente a través de Ejemplos de Estructura de Lewis
El enlace covalente es un tipo de enlace químico que se forma cuando dos átomos comparten electrones. Este fenómeno puede ser mejor comprendido a través de los Ejemplos de Estructura de Lewis, que representan la distribución de electrones en las moléculas. A continuación, se presentan algunos ejemplos que ilustran cómo se forman los enlaces covalentes y cómo se pueden representar con la estructura de Lewis.
Ejemplo 1: El Cloro (Cl2)
El cloro es un elemento que existe como una molécula diatómica (Cl2). Cada átomo de cloro tiene siete electrones en su capa de valencia y necesita un electrón más para completar su octeto. En la estructura de Lewis, se puede representar de la siguiente manera:
- Cada átomo de Cl tiene 7 electrones de valencia.
- Para formar el enlace covalente, un electrón de cada átomo se comparte.
- Esto da como resultado un par de electrones compartidos entre los dos átomos de Cl.
La representación de la estructura de Lewis para Cl2 se ve así:
“`
Cl:Cl
“`
Aquí, los dos puntos (:) representan el par de electrones compartidos.
Ejemplo 2: El Agua (H2O)
El agua es otro ejemplo clave donde los enlaces covalentes son evidentes. En esta molécula, el oxígeno se une a dos átomos de hidrógeno. La estructura de Lewis muestra lo siguiente:
- El oxígeno tiene seis electrones de valencia.
- Cada hidrógeno tiene un electrón de valencia.
- El oxígeno comparte un electrón con cada hidrógeno.
La representación de la estructura de Lewis para el agua es:
“`
H
|
H—O
“`
Aquí, el par de electrones compartidos se representa como líneas.
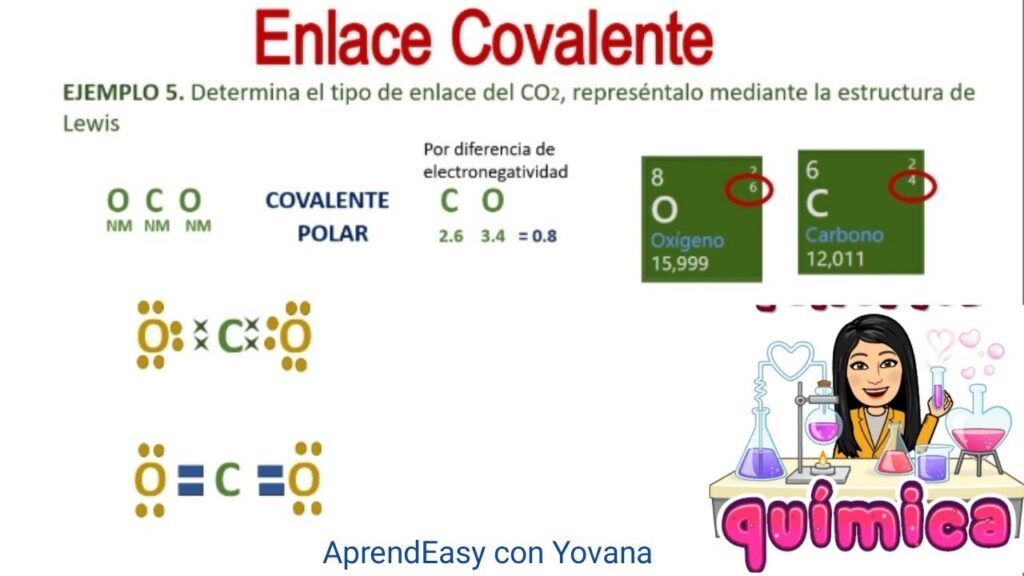
Ejemplo 3: El Dióxido de Carbono (CO2)
El dióxido de carbono es un ejemplo de un compuesto con enlaces dobles. En CO2, el carbono se une a dos átomos de oxígeno mediante enlaces covalentes dobles. La estructura de Lewis se representa de la siguiente manera:
- El carbono tiene cuatro electrones de valencia.
- Cada oxígeno tiene seis electrones de valencia.
- El carbono forma dos enlaces dobles con los dos átomos de oxígeno para completar su octeto.
La representación de la estructura de Lewis para CO2 es:
“`
O=C=O
“`
Los signos de igual (=) indican dos pares de electrones compartidos entre los átomos.
Ejemplo 4: El Metano (CH4)
El metano es un hidrocarburo simple donde un átomo de carbono se une a cuatro átomos de hidrógeno. La estructura de Lewis para el metano se describe de la siguiente manera:
- El carbono tiene cuatro electrones de valencia.
- Cada hidrógeno tiene un electrón de valencia.
- El carbono comparte un electrón con cada uno de los cuatro hidrógenos.
La representación de la estructura de Lewis para CH4 es:
“`
H
|
H—C—H
|
H
“`
En resumen, los ejemplos de estructuras de Lewis ofrecen una representación visual útil para comprender cómo los átomos se unen mediante enlaces covalentes, facilitando el estudio de la química molecular.
Definición y Características del Enlace Covalente
Concepto de Enlace Covalente
El enlace covalente es una interacción química que se forma cuando dos átomos comparten uno o más pares de electrones. Este tipo de enlace es fundamental en la formación de moléculas, dado que permite que los átomos alcancen una configuración electrónica más estable. A diferencia de los enlaces iónicos, donde los electrones son transferidos de un átomo a otro, en el enlace covalente ambos átomos contribuyen al par de electrones compartido.
Las características del enlace covalente incluyen su dirección y fuerza. Los enlaces covalentes pueden ser simples, dobles o triples, dependiendo de la cantidad de pares de electrones compartidos. Por ejemplo, el enlace entre dos átomos de hidrógeno (H₂) es un enlace covalente simple, mientras que el oxígeno (O₂) presenta un enlace covalente doble.
Propiedades de las Moléculas Covalentes
Las moléculas que poseen enlaces covalentes exhiben propiedades únicas que las distinguen de las compuestas por enlaces iónicos. Entre estas propiedades se encuentran:
- Punto de fusión y ebullición bajos: Generalmente, las sustancias covalentes tienen puntos de fusión y ebullición más bajos en comparación con las iónicas.
- Conductividad eléctrica: En estado sólido, estas moléculas no conducen electricidad debido a la falta de iones libres.
- Solubilidad: Muchas moléculas covalentes son solubles en solventes orgánicos, pero insolubles en agua.
Estas propiedades son fundamentales para entender el comportamiento de las sustancias en diferentes condiciones y aplicaciones.
Aplicación de la Estructura de Lewis en la Predicción de Enlaces Covalentes
Qué es la Estructura de Lewis
La estructura de Lewis es una representación gráfica que muestra cómo se distribuyen los electrones en una molécula. Esta representación es crucial para visualizar los enlaces covalentes formados entre los átomos. En la estructura de Lewis, los electrones de valencia se representan como puntos alrededor de los símbolos de los elementos, y los pares de electrones compartidos se indican mediante líneas.
La importancia de la estructura de Lewis radica en su capacidad para predecir la geometría molecular y las propiedades químicas. Al identificar cómo los electrones están dispuestos, los químicos pueden inferir cómo interactuarán las moléculas en diversas reacciones.
Ejemplos de Estructura de Lewis
Para ilustrar la utilidad de la estructura de Lewis, consideremos algunos ejemplos comunes:
- Agua (H₂O): En la estructura de Lewis, el oxígeno tiene dos pares de electrones no compartidos y forma enlaces simples con dos átomos de hidrógeno.
- Dióxido de carbono (CO₂): Aquí, el carbono forma dos enlaces dobles con dos átomos de oxígeno, lo que se representa con líneas entre el carbono y cada oxígeno en la estructura de Lewis.
- Metano (CH₄): El carbono comparte sus cuatro electrones de valencia formando cuatro enlaces simples con cuatro átomos de hidrógeno.
Estos ejemplos demuestran cómo la estructura de Lewis ayuda a visualizar los enlaces covalentes y su configuración electrónica.
Diferencias entre Enlace Covalente Polar e Im polar
Enlace Covalente Polar
El enlace covalente polar ocurre cuando dos átomos que se unen tienen diferentes electronegatividades. Esto significa que uno de los átomos atraerá más fuertemente los electrones compartidos, generando una distribución asimétrica de carga. Como resultado, se forma un dipolo eléctrico, donde un extremo de la molécula se vuelve parcialmente positivo y el otro parcialmente negativo.
Un ejemplo clásico de enlace covalente polar es el agua (H₂O), donde el oxígeno es más electronegativo que el hidrógeno, creando una molécula polar. Esta polaridad confiere al agua propiedades únicas, como su capacidad para disolver muchas sustancias.
Enlace Covalente No Polar
Por otro lado, el enlace covalente no polar se forma entre átomos de igual electronegatividad, como en el caso de las moléculas diatómicas homonucleares. En estos enlaces, los electrones se comparten equitativamente, lo que resulta en una distribución uniforme de carga.
Ejemplos de enlaces covalentes no polares incluyen el oxígeno (O₂) y el nitrógeno (N₂). Estas moléculas no presentan un dipolo, lo que implica que no interactúan tan fácilmente con moléculas polares.
Ejemplos Prácticos de Enlaces Covalentes en Compuestos Comunes
Compuestos Orgánicos
Los compuestos orgánicos son ricos en enlaces covalentes, especialmente en estructuras que contienen carbono. Un ejemplo emblemático es el etanol (C₂H₅OH), donde los átomos de carbono forman enlaces covalentes con hidrógeno y oxígeno. Estos enlaces son responsables de las propiedades físicas y químicas del etanol, como su capacidad para mezclarse con el agua.
La diversidad de compuestos orgánicos se debe a la capacidad del carbono para formar múltiples enlaces covalentes, resultando en una variedad de estructuras que pueden incluir cadenas lineales, ramificadas o cíclicas.
Compuestos Inorgánicos
En los compuestos inorgánicos también encontramos ejemplos de enlaces covalentes. Un caso notable es el ácido clorhídrico (HCl), donde el hidrógeno y el cloro comparten un par de electrones. La naturaleza covalente del enlace H-Cl es vital para entender su comportamiento en soluciones acuosas, donde se disocia en iones H⁺ y Cl⁻.
Además, el dióxido de carbono (CO₂) es otro ejemplo relevante. Su estructura covalente, que incluye enlaces dobles, es esencial para comprender su papel en procesos biológicos como la fotosíntesis y la respiración celular.
Conclusiones sobre el Enlace Covalente y la Estructura de Lewis
Importancia en la Química Moderna
El estudio del enlace covalente y la estructura de Lewis es fundamental en la química moderna. Comprender cómo se forman y comportan los enlaces covalentes permite a los científicos diseñar y sintetizar nuevos compuestos con propiedades específicas.
Estos conceptos son esenciales en campos como la bioquímica, farmacología y materiales avanzados, donde la manipulación de moléculas es clave para el desarrollo de nuevas tecnologías y tratamientos.
Perspectivas Futuras
A medida que la química avanza, la comprensión de los enlaces covalentes y sus representaciones continuará evolucionando. Nuevas técnicas y herramientas, como la espectroscopía y la química computacional, permitirán explorar con mayor profundidad las interacciones moleculares.
Con el continuo avance de la investigación, se espera que surjan nuevos modelos que complementen y expandan nuestro entendimiento actual del enlace covalente, proporcionando así una base más sólida para futuras innovaciones científicas.
Preguntas Frecuentes
¿Cuáles son algunos ejemplos de moléculas que presentan enlaces covalentes y su correspondiente estructura de Lewis?
Algunos ejemplos de moléculas que presentan enlaces covalentes son:
1. Agua (H₂O): La estructura de Lewis muestra un oxígeno central con dos pares de electrones compartidos con dos hidrógenos.
2. Dióxido de carbono (CO₂): Su estructura de Lewis tiene un carbono central unido a dos oxígenos mediante enlaces dobles.
3. Metano (CH₄): En su estructura de Lewis, el carbono está unido a cuatro hidrógenos por enlaces simples.
Estos ejemplos ilustran cómo los átomos comparten electrones para formar enlaces covalentes.
¿Cómo se representan los electrones compartidos en la estructura de Lewis de compuestos covalentes?
En la estructura de Lewis de compuestos covalentes, los electrones compartidos se representan mediante líneas que conectan los átomos. Cada línea representa un par de electrones compartidos. Por ejemplo, en el caso del agua (H₂O), el oxígeno está unido a dos hidrógenos por dos líneas, indicando que comparte un par de electrones con cada uno.
¿Qué diferencias existen en la representación de la estructura de Lewis entre moléculas simples y compuestas?
La representación de la estructura de Lewis para moléculas simples, como el agua (H₂O), muestra los enlaces entre átomos y los pares de electrones libres de manera clara y directa. En cambio, las moléculas compuestas, como el ácido sulfúrico (H₂SO₄), requieren una representación más compleja, donde se deben mostrar múltiples enlaces y la disposición de varios átomos, lo que puede incluir estructuras resonantes. Por lo tanto, la complejidad y el número de átomos son las principales diferencias entre ambas representaciones.
¿Cómo se pueden utilizar los ejemplos de estructuras de Lewis para predecir la geometría molecular de compuestos covalentes?
Los ejemplos de estructuras de Lewis son fundamentales para predecir la geometría molecular de compuestos covalentes. Al dibujar la estructura de Lewis, se pueden identificar los pares de electrones y los átomos centrales. Luego, utilizando la teoría de repulsión de pares de electrones (VSEPR), se puede determinar la geometría molecular basándose en la disposición espacial de estos pares. Por ejemplo, si un átomo tiene dos pares de electrones libres y dos enlaces, la geometría será angular.
En conclusión, el enlace covalente y la estructura de Lewis son fundamentales en la comprensión de la química molecular. A través de los ejemplos presentados, se evidencia su aplicación en diversas moléculas. Te invitamos a compartir este contenido y seguir explorando nuestros artículos para profundizar más en estos temas.