¿Te has preguntado cómo ocurren las reacciones químicas de sustitución doble? Este fascinante proceso, donde dos compuestos intercambian sus componentes, es fundamental en la química. En este artículo, exploraremos ejemplos concretos y aplicaciones prácticas que ilustran este fenómeno. A través de reacciones como la formación de precipitados y la liberación de gases, descubriremos el trasfondo teórico y experimental que las rodea.
Prepárate para sumergirte en un mundo donde los elementos se transforman y dan lugar a nuevos compuestos. ¡Sigue leyendo para descubrir más!
Contenido
- ### Explorando Ejemplos de Reacciones Químicas de Sustitución Doble: Procesos y Aplicaciones en la Química
- Concepto de Reacciones de Sustitución Doble
- Ejemplos Comunes de Reacciones de Sustitución Doble
- Condiciones que Favorecen las Reacciones de Sustitución Doble
- Aplicaciones Prácticas de las Reacciones de Sustitución Doble
- Preguntas Frecuentes
### Explorando Ejemplos de Reacciones Químicas de Sustitución Doble: Procesos y Aplicaciones en la Química
Las reacciones químicas de sustitución doble son un tipo de reacción en la que dos compuestos intercambian componentes para formar nuevos productos. Este proceso es fundamental en la química, ya que permite la formación de diversas sustancias útiles en diferentes aplicaciones industriales y biológicas.
Ejemplos de Reacciones de Sustitución Doble se pueden observar en varias reacciones típicas:
- Reacciones de Halogenuros: Un ejemplo clásico es la reacción entre el cloruro de sodio (NaCl) y el nitrato de plata (AgNO3), donde se produce cloruro de plata (AgCl), un precipitado blanco, y nitrato de sodio (NaNO3).
- Reacciones Ácido-Base: Cuando el ácido clorhídrico (HCl) reacciona con el hidróxido de sodio (NaOH), se forma agua (H2O) y cloruro de sodio (NaCl), ilustrando una reacción de neutralización en la que se intercambian iones.
- Reacciones de Carbonatos: La reacción del carbonato de calcio (CaCO3) con el ácido clorhídrico (HCl) produce cloruro de calcio (CaCl2), agua (H2O) y dióxido de carbono (CO2), demostrando cómo los carbonatos pueden liberar gas al reaccionar con ácidos.
Aplicaciones de las Reacciones de Sustitución Doble son amplias y variadas en el campo de la química:
- Síntesis de Materiales: Estas reacciones son fundamentales en la síntesis de nuevos compuestos químicos que son esenciales en la fabricación de productos farmacéuticos, plásticos y otros materiales industriales.
- Tratamiento de Aguas Residuales: Se utilizan en procesos de purificación de aguas, como la eliminación de metales pesados mediante la precipitación de compuestos insolubles.
- Producción de Alimentos: En la industria alimentaria, las reacciones de sustitución doble se aplican para modificar características de los alimentos, como el sabor y la textura, a través de la formación de nuevos compuestos.
En términos de mecanismos, estas reacciones generalmente ocurren en un medio acuoso y son impulsadas por la formación de un producto insoluble o la liberación de un gas. Los reactivos intercambian sus iones, lo que permite que la reacción avance hacia la formación de productos más estables.
La comprensión de las reacciones de sustitución doble es crucial para los químicos, ya que permite no solo la predicción de productos, sino también la manipulación de condiciones para obtener rendimientos óptimos en diversas aplicaciones.
Concepto de Reacciones de Sustitución Doble
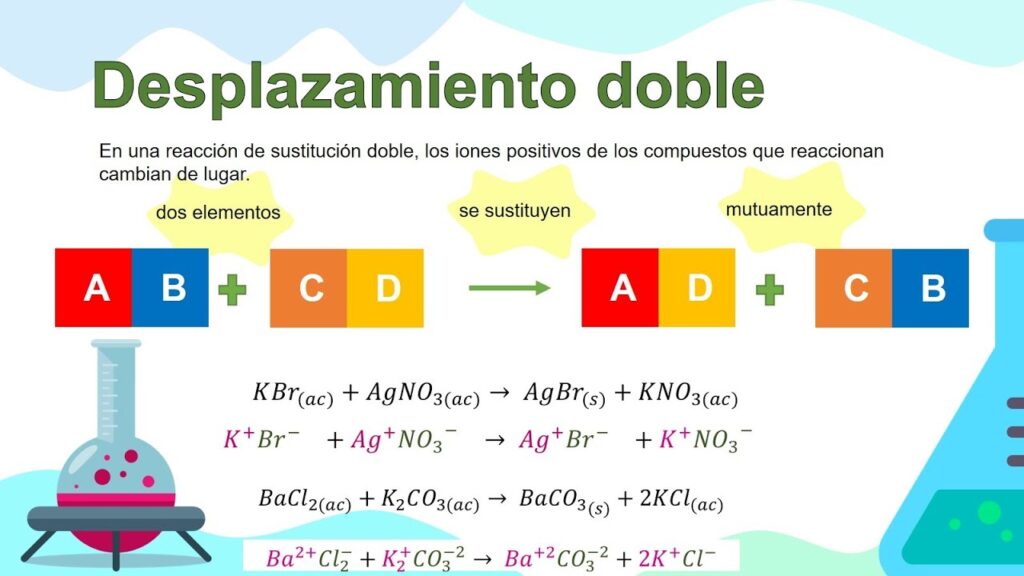
Las reacciones de sustitución doble, también conocidas como reacciones de intercambio, son un tipo fundamental de reacciones químicas. En este tipo de reacciones, dos compuestos intercambian sus componentes, dando lugar a la formación de nuevos productos. Este proceso se puede representar con la siguiente ecuación general:
AB + CD → AD + CB
En esta ecuación, A y C son los cationes, mientras que B y D son los aniones. Es importante mencionar que estas reacciones suelen ocurrir en soluciones acuosas y son comunes en la química inorgánica.
Mecanismo de la Reacción
El mecanismo de las reacciones de sustitución doble generalmente implica la disociación de los reactivos en iones. Cuando dos compuestos iónicos se mezclan en solución, cada compuesto se separa en sus respectivos iones. Por ejemplo, al mezclar cloruro de sodio (NaCl) y nitrato de plata (AgNO₃), se produce una reacción donde el Na⁺ se combina con NO₃⁻ y Ag⁺ se combina con Cl⁻.
- Disociación de los compuestos en iones.
- Intercambio de iones entre los compuestos.
- Formación de nuevos compuestos a partir de los iones intercambiados.
Es fundamental que los productos formados sean menos solubles o precipiten en comparación con los reactivos originales para que la reacción ocurra de manera notable.
Ejemplos Comunes de Reacciones de Sustitución Doble
Existen numerosos ejemplos de reacciones de sustitución doble en la práctica química. Estos ejemplos son ilustrativos de cómo distintos compuestos interactúan entre sí, y son esenciales para entender procesos más complejos en química.
- Reacción entre cloruro de sodio y nitrato de plata: NaCl + AgNO₃ → AgCl↓ + NaNO₃
- Reacción entre sulfato de cobre(II) y carbonato de sodio: CuSO₄ + Na₂CO₃ → CuCO₃↓ + Na₂SO₄
- Reacción entre ácido clorhídrico y carbonato de calcio: HCl + CaCO₃ → CaCl₂ + CO₂↑ + H₂O
Estos ejemplos no solo demuestran el principio de sustitución doble, sino que también ilustran la formación de precipitados o gases, lo cual es un indicativo de que ha ocurrido una reacción química.
Importancia de los Productos Formados
Los productos de las reacciones de sustitución doble pueden tener propiedades muy diferentes a las de los reactivos originales. En muchos casos, estos productos son más útiles en aplicaciones industriales y de laboratorio. Por ejemplo, el cloruro de plata (AgCl) formado en la primera reacción es un compuesto fotográfico utilizado en la producción de películas y en la fotografía antigua.
Además, algunos productos resultantes pueden ser tóxicos o peligrosos, lo que requiere un manejo adecuado. Por lo tanto, es esencial que los químicos comprendan no sólo cómo llevar a cabo estas reacciones, sino también las propiedades y riesgos asociados con los productos generados.
Condiciones que Favorecen las Reacciones de Sustitución Doble
Para que una reacción de sustitución doble ocurra eficientemente, deben cumplirse ciertas condiciones. Estas incluyen la formación de un producto insoluble, la generación de gas o la neutralización de un ácido y una base.
Factores que Influyen en la Reacción
Algunos de los factores que pueden influenciar la efectividad de una reacción de sustitución doble incluyen:
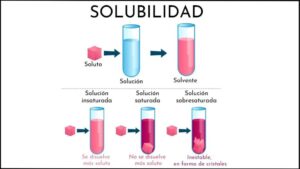
- Solubilidad: La mayoría de estas reacciones ocurren cuando uno de los productos es insoluble en agua, lo que provoca la precipitación y, por lo tanto, el desplazamiento de la reacción hacia la derecha.
- Concentración de Reactivos: Aumentar la concentración de los reactivos puede aumentar la velocidad de la reacción, facilitando el intercambio de iones.
- Temperatura: Las reacciones suelen ser más rápidas a temperaturas más altas debido al aumento de energía cinética de las moléculas involucradas.
Es importante tener en cuenta que la combinación de estos factores puede optimizar el rendimiento de las reacciones de sustitución doble en diversos contextos químicos.
Aplicaciones Prácticas de las Reacciones de Sustitución Doble
Las reacciones de sustitución doble tienen muchas aplicaciones prácticas en diversas áreas de la química y la industria. Desde la producción de compuestos químicos hasta procesos de purificación, su utilidad es inmensa.
Usos en la Industria Química
En la industria, estas reacciones son fundamentales para la fabricación de productos químicos. Por ejemplo, la síntesis de sales inorgánicas y la producción de pigmentos son solo algunas de las aplicaciones que dependen de estas reacciones.
- Producción de Fertilizantes: Muchas reacciones de sustitución doble se utilizan para producir fertilizantes a través de la combinación de diferentes compuestos químicos.
- Tratamiento de Aguas Residuales: Se emplean para eliminar metales pesados y otros contaminantes a través de la precipitación de compuestos no solubles.
- Laboratorios de Análisis Químico: Se utilizan en diversas pruebas analíticas y en la preparación de soluciones estándar.
En resumen, las reacciones de sustitución doble son un pilar fundamental en la química, con un amplio rango de aplicaciones prácticas que reflejan su importancia en la ciencia y la industria.
Preguntas Frecuentes
¿Cuáles son los ejemplos más representativos de reacciones de sustitución doble en la química orgánica e inorgánica?
Los ejemplos más representativos de reacciones de sustitución doble son:
1. En química inorgánica: la reacción entre el cloruro de sodio y el nitrato de plata, donde se forma nitrato de sodio y cloruro de plata:
[
text{NaCl} + text{AgNO}_3 rightarrow text{NaNO}_3 + text{AgCl}
]
2. En química orgánica: la reacción entre un halogenuro de alquilo y una solución de hidróxido de sodio, donde se obtiene un alcohol:
[
text{R-X} + text{NaOH} rightarrow text{R-OH} + text{NaX}
]
Estos ejemplos son clave para entender cómo los compuestos intercambian elementos en soluciones.
¿Cómo se equilibran las ecuaciones químicas de las reacciones de sustitución doble?
Para equilibrar las ecuaciones químicas de las reacciones de sustitución doble, se deben seguir estos pasos:
1. Escribir la ecuación no equilibrada: Anotar los reactivos y productos.
2. Identificar los compuestos: Asegurarse de que todos los compuestos estén correctamente representados.
3. Contar los átomos: Hacer una lista de los átomos de cada elemento en reactivos y productos.
4. Ajustar coeficientes: Modificar los coeficientes delante de los compuestos para igualar el número de átomos de cada elemento en ambos lados.
5. Verificar el equilibrio: Comprobar que el número total de átomos sea el mismo en reactivos y productos.
Por ejemplo, en la reacción de NaCl + AgNO3 → NaNO3 + AgCl, se puede equilibrar observando que ya hay un equilibrio en la cantidad de átomos de cada elemento.
¿Qué condiciones experimentales son necesarias para llevar a cabo reacciones de sustitución doble efectivas?
Para llevar a cabo reacciones de sustitución doble efectivas, se requieren las siguientes condiciones experimentales:
1. Solubilidad de los reactivos: Al menos uno de los productos debe ser insoluble o debe formar un gas.
2. Concentración adecuada: Los reactivos deben estar presentes en cantidades suficientes para favorecer la reacción.
3. Temperatura controlada: Mantener una temperatura adecuada que favorezca la velocidad de reacción sin descomponer los reactivos.
4. Agitación: Facilitar la mezcla de los reactivos para aumentar la probabilidad de colisiones efectivas.
Estas condiciones aseguran una mayor eficacia en la reacción de sustitución doble.
¿Cuál es la importancia de las reacciones de sustitución doble en procesos industriales y biológicos?
Las reacciones de sustitución doble son fundamentales en procesos industriales y biológicos porque permiten la transformación de compuestos químicos de manera eficiente. Por ejemplo, en la industria química, estas reacciones se utilizan para producir sales a partir de ácidos y bases, mientras que en los sistemas biológicos, facilitan la metabolización de nutrientes y la eliminación de desechos. Esto optimiza la producción y el mantenimiento de la vida en organismos.
En conclusión, los ejemplos de reacciones químicas de sustitución doble ilustran la complejidad y belleza de la química. Comprender estos procesos es fundamental para diversas aplicaciones científicas. Te invitamos a compartir este contenido y a seguir explorando más sobre el fascinante mundo de la química en nuestros próximos artículos.